Forschung & Entwicklung
AMW zeichnet sich durch eine innovative Forschungs- und Entwicklungsstrategie aus, die auf Spitzentechnologie und Know-how fußt. Von der präklinischen Entwicklung bis zum Upscaling in die klinische GMP-Fertigung wird jeder Entwicklungsschritt sorgfältig geplant, um überlegene Lösungen für die Arzneimittel-Verabreichung zu entwickeln. Patientinnen und Patienten stehen im Mittelpunkt, wenn durch die Kombination von einzigartiger Technologie mit pharmazeutischer und biotechnologischer Expertise innovative Therapien geschaffen werden.
In der modernen Medizin bestehen komplexe Probleme, die sowohl für Patientinnen und Patienten als auch für Gesundheitsfachkräfte eine erhebliche Belastung darstellen. Von komplizierten Verabreichungsprotokollen bis hin zu schwierigen Dosiskontrollen und der oft unzureichenden Wirksamkeit aktueller Behandlungen – es existieren signifikante Lücken in der Versorgung, die adressiert werden müssen. Biologisch abbaubare Implantate mit kontrollierter Wirkstoffabgabe zeigen sich als innovative Lösung, die viele dieser ungedeckten klinischen Bedürfnisse erfüllt, und bringen dabei eine Reihe von Schlüsselvorteilen mit sich:
- Gewährleistung eines stabilen und anhaltenden therapeutischen Wirkstoffspiegels des aktiven pharmazeutischen Wirkstoffs
- Ein Produkt, das über mehrere Wochen oder Monate Wirkstoff freisetzt und somit die Notwendigkeit wiederholter Anwendungen minimiert
- Effiziente Lösung für die Herausforderung, eine hohe Therapie-Adhärenz zu erreichen
- Prädestiniert für die Anwendung in Körperbereichen, die von der systemischen Blutversorgung schwer zu erreichen sind
- Prävention von unbeabsichtigten oder vorsätzlichen Überdosierungen
Der AMW-Weg
Bei AMW beruht der Entwicklungsprozess auf fundierter Expertise und einer reichen Historie an Erfahrungen, die sich von den Anfängen der Formulierungsentwicklung bis hin zur klinischen und kommerziellen Herstellung erstreckt. Mit einem breiten Spektrum an Kompetenzen präsentiert sich AMW als Ihre „Single Source“-Einrichtung, die bereits bei der Entwicklung eines optimalen Formulierungsdesigns, basierend auf biologisch abbaubaren polymeren Matrizen, beginnt. Chemische Bestandteile, insbesondere Polymere, werden sorgfältig ausgewählt und zu Prototyp-Matrizes entwickelt, die perfekt mit einer Wirkstoff-Integration durch Schmelzextrusion harmonieren. Hierbei kann der aktive pharmazeutische Wirkstoff innerhalb der Matrix optimal verteilt oder teilweise bzw. vollständig gelöst werden, um eine maximale therapeutische Wirksamkeit zu gewährleisten. Die Arzneimittelmatrix wird in einem sorgfältig konzipierten Entwicklungsprozess weitergeführt, der sich über verschiedene technische Phasen erstreckt. Jede Phase zielt darauf ab, spezifische Optimierungen vorzunehmen, darunter:
- Einschränkung der molekularen Mobilität des Wirkstoffs, um eine kontrollierte Freisetzung zu erreichen
- Mischbarkeitstests, um Löslichkeitsproblemen entgegenzuwirken
- Robuster Extrusionsprozess mit reproduzierbaren Ergebnissen, der thermische Belastungen von Polymer und Wirkstoff minimiert
- Festkörpercharakterisierung des Implantats
- Ergänzt durch maßgeschneiderte, hochmoderne chemische Analysen
Nach der galenischen Entwicklung nutzt AMW standardisierte und effiziente Verfahren, um den Übergang zu einer internen, qualitätszertifizierten GMP-Produktionsanlage zu vollziehen. Diese Anlage ist bestens gerüstet, um sowohl die klinische als auch die anschließende kommerzielle Chargenproduktion durchzuführen.
Quality by Design
Bei AMW stehen Forschung und Entwicklung im Mittelpunkt, ein Beleg unserer festen Verpflichtung, in diesem Bereich eine Vorreiterrolle zu spielen. Unser auf wissenschaftlichen Standards beruhender Ansatz ist ein Paradebeispiel für die Philosophie der „Quality by Design“ (QbD).
Dieses Engagement garantiert, dass jede Phase der Projekteinführung den internationalen Standards für Exzellenz entspricht. Das versierte F&E-Team von AMW definiert und steuert die analytischen Prozesse und Protokolle, wobei diverse Prozess-Analytik-Technologien (PAT) zielführend integriert werden:
Materialcharakterisierung und Formulierung
- Mikroskopische Bildanalyse: Ein wesentliches Werkzeug zur Bewertung der morphologischen Aspekte der Formulierung. Dieser Prozess ermöglicht eine tiefgehende Untersuchung der mikroskopischen, strukturellen Eigenschaften, unterstützt die Optimierung der Formulierung und ermöglicht Vorhersagen zur Freisetzungskinetik durch präzise Bestimmung und Quantifizierung der Partikelgrößenverteilung und anderer relevanter Faktoren.
- ATR-FTIR-Spektroskopie: Eine essenzielle Technik zur Aufklärung der chemischen Zusammensetzung von Materialien. Sie gewährt eine detaillierte Untersuchung der molekularen Strukturen und Interaktionen, welche entscheidend sind, um die Verteilung und Homogenität der verschiedenen Komponenten innerhalb der Formulierung zu gewährleisten.
- GPC (Gelpermeationschromatographie): Eine zentrale Methode zur Analyse der Molekulargewichtsverteilung der Polymere in der Formulierung. Diese Technik liefert grundlegende Erkenntnisse über die potenzielle, ungewollte Degradation der Polymere sowie zur Prozessstabilität.
- DSC (Differential-Scanning-Kalorimetrie): Ein zentrales Instrument zur Erfassung der thermischen Eigenschaften der Materialien, das wichtige Informationen zur Glasübergangstemperatur der Polymerkomponenten und zur Löslichkeit des aktiven pharmazeutischen Wirkstoffs in der Polymermatrix liefert, wodurch der Herstellungsprozess entscheidend optimiert werden kann.
- Rheologie: Eine Technik, die die Fließeigenschaften der Formulierungen analysiert, wodurch das Prozessfenster für die Extrusion definiert und ein gleichmäßiger Drehmomentverlauf während der Extrusion sichergestellt wird, was zu einer höheren Produktqualität beiträgt.
Analytische Prüfung
- HPLC (High Pressure Liquid Chromatography)/UPLC (Ultra High Performance Liquid Chromatography) in Kombination mit UV-, RI-, Fluoreszenz- und MS-Detektionsmethoden ist ein unverzichtbares Instrument für die quantitative Analyse des aktiven pharmazeutischen Wirkstoffs und potenzieller Abbauprodukte in pharmazeutischen Formulierungen. Dieses Verfahren nimmt eine Schlüsselposition bei der Bestimmung der Freisetzungskinetik sowie der Überwachung von Gehalt und Reinheit des Implantats ein.
- HS-GC (Headspace-Gaschromatographie): Eine Technik, die in unserem Labor zur Verfügung steht und sich auf die Analyse flüchtiger Verbindungen in der Formulierung konzentriert. Obwohl GC im Vergleich zu GPC und HPLC nur in speziellen Fällen bei der Untersuchung von biologisch abbaubaren Implantaten verwendet wird, bleibt es ein wichtiges Instrument zur Gewährleistung der Stabilität und Sicherheit des Produkts in speziellen Szenarien.
- Coulometrische Wasserbestimmung: Eine Methode, die sich speziell auf die Analyse des Wassergehalts in den Formulierungen fokussiert. Der Wassergehalt ist ein kritischer Faktor, der sowohl die Langzeitstabilität des Produkts als auch die Stabilität hydrolyseempfindlicher Polymere während der Extrusion maßgeblich beeinflusst.
Produktprüfung und Validierung
- Mechanische Materialprüfung: Ein wichtiger Prozess zur Beurteilung der mechanischen Eigenschaften des Produkts, der detaillierte Informationen zum Verhalten des Produkts unter verschiedenen physischen Belastungen liefert, wie sie bei der Handhabung des Implantats oder dem Konfektionieren auftreten können.
- In-vitro-Freisetzungstests gemäß Ph. Eur., USP sowie eigenen Methoden: Diese Tests, die so weit wie möglich nach regulatorischen Vorgaben durchgeführt werden, sind entscheidend für die Erfassung der Freisetzungskinetik der Wirkstoffe. Bei Bedarf können die Tests jedoch modifiziert werden, um den besonderen Eigenschaften biologisch abbaubarer Polymere gerecht zu werden, was zentral für die Bewertung der potenziellen klinischen Produktwirksamkeit ist.
- ICH-Stabilitätsstudien (alle Klimazonen): Diese Studien sind entscheidend für die Bestimmung der Produktstabilität unter verschiedenen Umweltbedingungen der unterschiedlichen Wirtschaftsräume.
Bei AMW ermöglicht die breite Palette der zur Verfügung stehenden analytischen Technologien eine kontinuierliche und individuelle Methodenentwicklung, gepaart mit sorgfältiger Validierung, um den einzigartigen Anforderungen jedes Projekts gerecht zu werden. Mit den Lizenzen für den Umgang mit kontrollierten Substanzen ermöglichen wir die Umsetzung neuer F&E-Initiativen, unterstützt durch umfangreiche Ressourcen und die strikte Einhaltung regulatorischer Standards. Unser Engagement konzentriert sich darauf, Innovationen voranzutreiben, sei es durch eigene Entwicklungen oder durch die Förderung kollaborativer Partnerschaften.
Schmelzextrusion
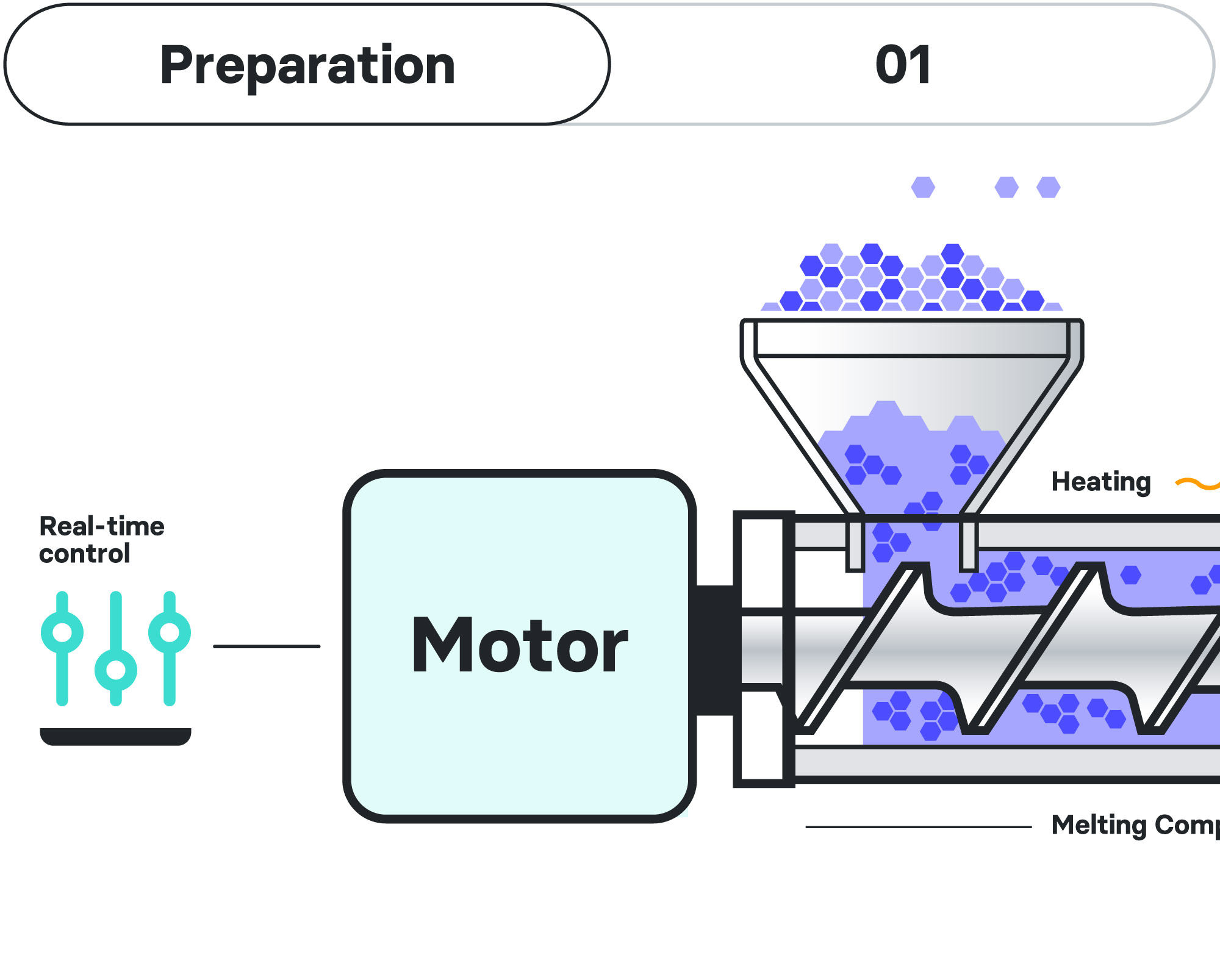
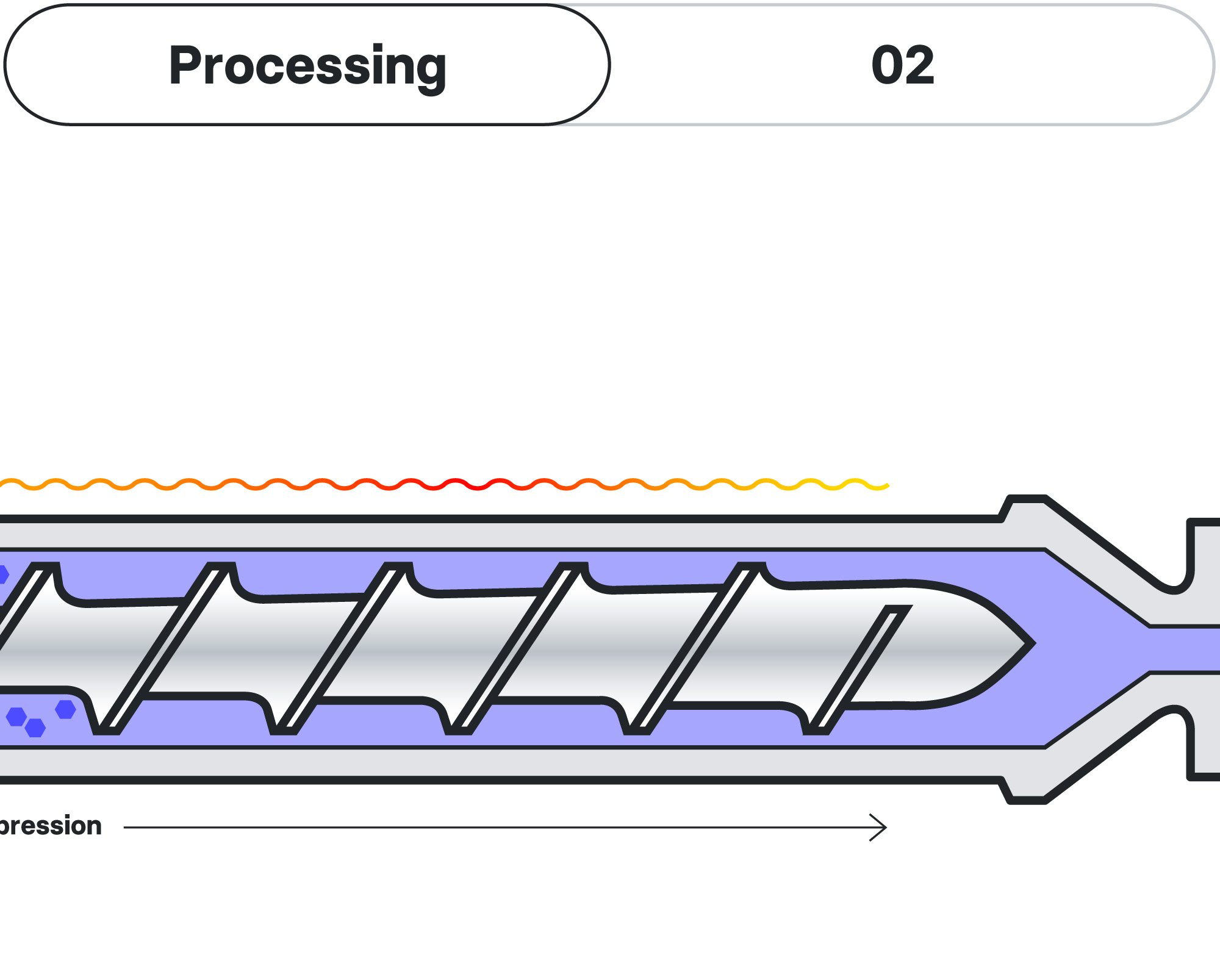
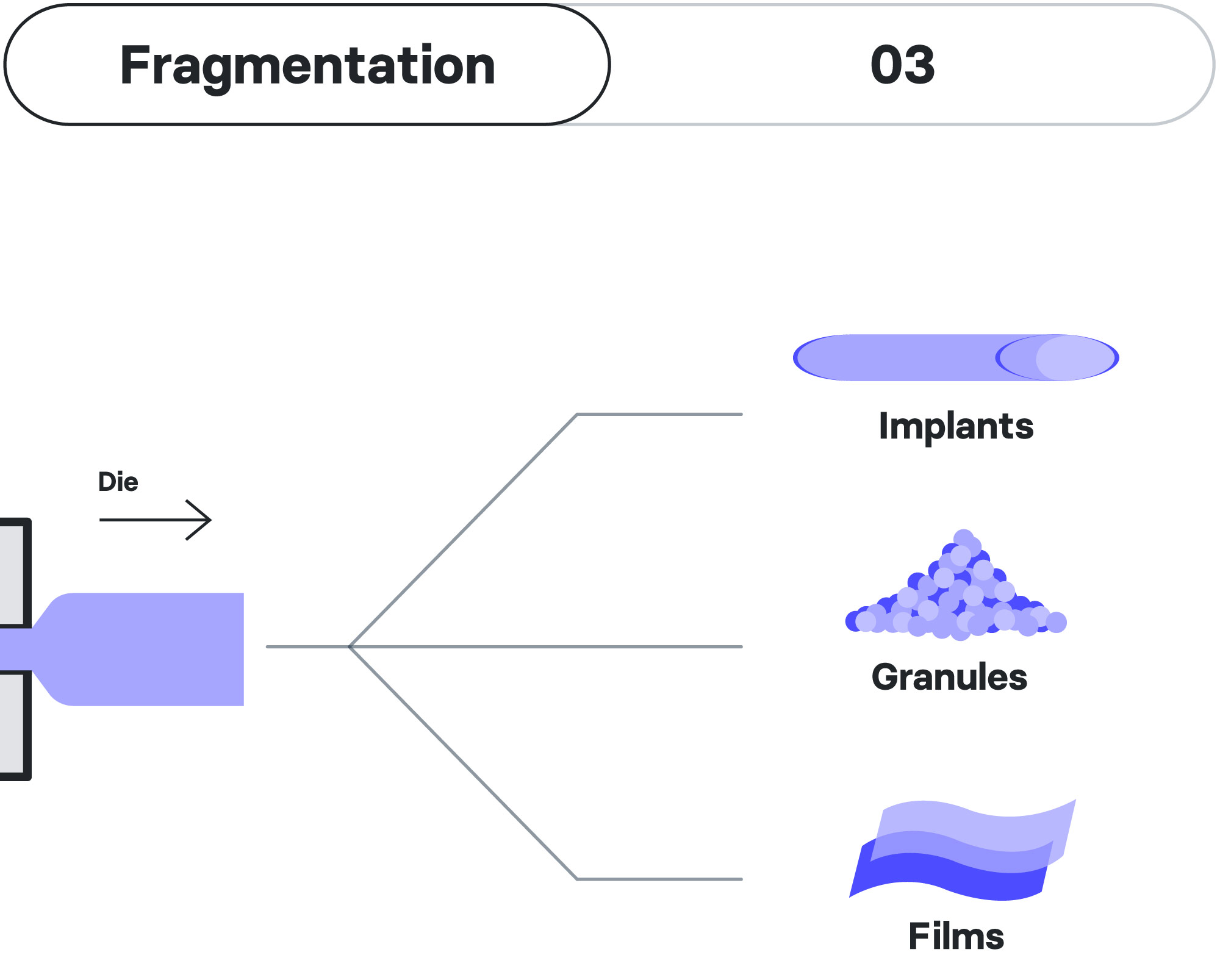
Die biologisch abbaubaren Implantate von AMW werden mit Hilfe der Schmelzextrusion-Plattformtechnologie gefertigt, einer wichtigen Methode in den Bereichen pharmazeutische Formulierung, Produktentwicklung und Herstellung. Diese Methode ist besonders geeignet, um eine hochwertige, langanhaltende Arzneimittelabgabe in einem gut skalierbaren Prozess zu ermöglichen. In einem optimierten Verfahren verschmilzt eine pulverförmige Mischung aus Polymeren mit einem spezifischen Wirkstoff, was in den meisten Fällen zu einer amorphen, festen Dispersion des Moleküls innerhalb der neu formulierten Matrix führt. Die Schmelze wird unter Druck in die gewünschte, meist stäbchenförmige Form gebracht und in die gewünschte Länge geschnitten.
Durch dieses Verfahren wird die Löslichkeit des aktiven Bestandteils erhöht, der in seiner kristallinen Form normalerweise nur begrenzt wasserlöslich wäre. Um eine graduelle und kontrollierte Freisetzung zu gewährleisten, werden die Implantate sowohl in der Zusammensetzung als auch in der Struktur kundengerecht designt. Diese sorgfältige Optimierung garantiert einen vorhersagbaren und reproduzierbaren hydrolytischen Abbau der Matrix, idealerweise mit einer linearen Freisetzungskinetik des Wirkstoffs innerhalb des therapeutischen Fensters.
Die Schmelzextrusion hat sich als eine anerkannte Technik in der pharmazeutischen Entwicklung etabliert, insbesondere bei der Erstellung von Formulierungen für die lokale Arzneimittelabgabe mit anhaltender Wirkung.
Vorteile der Schmelzextrusion gegenüber anderen Formulierungstechniken
- Verbesserte Löslichkeit und Bioverfügbarkeit: Durch die Anwendung der Schmelzextrusion lässt sich die Löslichkeit von schwer wasserlöslichen Wirkstoffen optimieren, was potenziell zu einer verbesserten Bioverfügbarkeit im Organismus führt.
- Kontinuierliche Fertigung: Schmelzextrusion ist ideal für die kontinuierliche Fertigung geeignet, was nicht nur die Möglichkeit einer Kostensenkung in der Herstellung bietet, sondern auch eine konstante Produktqualität und eine vereinfachte Skalierung vom Forschungsstadium zur kommerziellen Fertigung ermöglicht.
- Keine Lösungsmittel: Im Gegensatz zu anderen Techniken benötigt Schmelzextrusion normalerweise keine Lösungsmittel, was den Formulierungsprozess vereinfacht und die Technik umweltfreundlicher macht.
- Flexibilität bei der Formulierung: Schmelzextrusion kann zur Herstellung einer breiten Palette von Darreichungsformen, einschließlich Tabletten, Kapseln und Filmen, verwendet werden, was Flexibilität bei der Formulierungsentwicklung bietet.
- Präzise Kontrolle der Freisetzungsrate: Das Verfahren erlaubt eine genaue Steuerung der Freisetzungsrate der aktiven Inhaltsstoffe, die durch eine sorgfältige Auswahl der Polymere und eine wissenschaftlich fundierte Optimierung der Prozessparameter erreicht wird.
- Gleichmäßige Dispersion des Wirkstoffs: Mittels Schmelzextrusion lassen sich Formulierungen mit einer homogenen Verteilung des aktiven pharmazeutischen Wirkstoffs erzeugen. Dies ermöglicht eine kontrollierte Freisetzung und kann so das Auftreten von Nebenwirkungen durch Dosisspitzen minimieren.
- Komplexe Matrix-Formulierungen: Die Schmelzextrusions-Technik erlaubt die Entwicklung komplexer Matrix-Formulierungen, die mehrere Wirkstoffe mit unterschiedlichen Freisetzungsprofilen integrieren können. Dies stellt einen signifikanten Vorteil bei der Entwicklung von Kombinationstherapien dar.
- Stabilität: Formulierungen, die mittels Schmelzextrusion erzeugt werden, zeichnen sich häufig durch hohe Stabilität aus. Dies schützt empfindliche aktive pharmazeutische Wirkstoffe vor Abbau über die Haltbarkeitsdauer des Produkts.
- Regulatorische Akzeptanz: Schmelzextrusion genießt bei der Zulassung von Arzneimitteln eine hohe Akzeptanz seitens der Regulierungsbehörden, was den Genehmigungsprozess potenziell vereinfachen kann. Dies bietet einen Vorteil gegenüber Produkten, die durch technisch komplexere und schwerer zu überwachende Verfahren hergestellt werden.
Einschränkungen
Trotz ihrer zentralen Rolle in der pharmazeutischen Entwicklung ist die Schmelzextrusion nicht ohne Herausforderungen, insbesondere wenn es um die Eignung aktiver pharmazeutischer Inhaltsstoffe geht. Im Folgenden werden einige der potenziellen Einschränkungen und Anforderungen für Wirkstoffe im Kontext der Schmelzextrusion beschrieben:
- Thermische Stabilität: Wirkstoffe, die thermisch empfindlich sind, könnten im Extrusionsprozess degradieren. Durch eine sorgfältige Auswahl der Komponenten und gezielte Voruntersuchungen können die Prozessbedingungen jedoch so gestaltet werden, dass sie möglichst schonend für den Wirkstoff sind.
- Komplexität in der Formulierung: Die Erstellung von Formulierungen mit exakt definierten Freisetzungsprofilen für Arzneimittel kann oftmals komplex sein und erfordert eine umfassende Forschungs- und Entwicklungsarbeit, um die Charakteristika der Formulierung zu optimieren.
- Physische und chemische Wechselwirkungen: Während des Extrusionsprozesses können physikalische und chemische Interaktionen zwischen dem aktiven pharmazeutischen Wirkstoff und den Matrix-Polymeren stattfinden. Diese Interaktionen könnten potenziell die Stabilität oder die Freisetzungscharakteristika des fertigen Produkts beeinträchtigen.
- Kostenfaktoren: Die Investitionskosten für eine Extrusionslinie können erheblich sein, vor allem wenn man die hochspezialisierten Maschinen und die notwendigen analytischen Instrumente in Betracht zieht. Zudem können die Ausgaben steigen, falls spezialisierte Polymere in der Formulierung zum Einsatz kommen.
- Begrenzt auf bestimmte Wirkstoffe: Aufgrund ihrer physikalischen und chemischen Eigenschaften sind nicht alle aktiven pharmazeutischen Wirkstoffe für die Schmelzextrusion geeignet. Die Identifizierung kompatibler Polymere für spezifische Wirkstoffe kann eine anspruchsvolle Aufgabe darstellen.
Anforderungen an den Wirkstoff
- Thermische Stabilität: Der Wirkstoff sollte eine gute thermische Stabilität aufweisen, um den während des Extrusionsprozesses üblicherweise auftretenden hohen Temperaturen ohne Zerfall standzuhalten.
- Kompatibilität mit Polymeren: Der aktive pharmazeutische Wirkstoff sollte mit den in der Formulierung verwendeten Polymeren und anderen Hilfsstoffen kompatibel sein und seine Stabilität sowie Wirksamkeit durch den gesamten Produktionsprozess hindurch bewahren.
- Ausreichende Dispergierbarkeit: In der Schmelzextrusion eingesetzte aktive pharmazeutische Wirkstoffe sollten gut in der polymeren Matrix dispergierbar sein, um eine homogene Verteilung und effiziente Freisetzung aus der Formulierung sicherzustellen.
- Partikelgröße: Bei amorphen festen Dispersionen ist die Partikelgröße ein entscheidender Faktor, der maßgeblich die Erzielung eines spezifischen Arzneimittelfreisetzungsprofils beeinflusst. Die optimale Partikelgröße wird in Voruntersuchungen festgelegt und sollte im Verlauf der gesamten Prozesskette nur in einem kontrollierbaren und reproduzierbaren Umfang variieren.
- Kristallinität: Die Kristallinität und die polymorphen Formen des aktiven pharmazeutischen Wirkstoffs können Einfluss auf dessen Freisetzungsverhalten haben. In bestimmten Fällen kann es erforderlich sein, die Wirkstoffe im Vorfeld zu prozessieren, um die gewünschte polymorphe Form zu erhalten.
Mit nahezu zwei Jahrzehnten Expertise im Umgang mit diesen Herausforderungen und Anforderungen verfügt AMW über überlegenes Know-how, um die Schmelzextrusion zur Entwicklung und Herstellung von pharmazeutischen Produkten mit optimierten Eigenschaften einzusetzen.
Vielseitige Innovations- & Kooperationsmöglichkeiten
Bei AMW wird der Kurs der Innovation durch vielseitige Forschungs- und Entwicklungsoptionen sowie durch agile Geschäftsmodelle geprägt. Unsere Kernkompetenz liegt in einer breit gefächerten Technologiepalette, die eine Vielzahl von Produkten für diverse klinische Anwendungsbereiche umfasst. Hierbei setzt AMW auf die Integration verschiedener therapeutisch aktiver Komponenten in eine passende Matrix mittels Schmelzextrusion. Diese Schlüsseltechnologie bildet die Grundlage für eine robuste Plattform, die zahlreiche Kooperations- und Partnerschaftsmöglichkeiten mit Unternehmen aus den Bereichen Pharmazie, Biotechnologie und Medizintechnik unter verschiedenen flexiblen Rahmenbedingungen ermöglicht.
Inhouse-Innovation
Ein wesentlicher Antrieb für unsere Eigenentwicklungen ist die Zielsetzung, bisher ungedeckte klinische Bedürfnisse im Segment der lokalen Arzneimittelverabreichung zu erfüllen. Hierbei fokussieren sich die Teams von AMW auf die Eigenentwicklung innovativer Medikamentenabgabesysteme. Diese Initiativen haben das Ziel, innovative Therapieoptionen für die lokale Wirkstoffabgabe mit kontrollierten Freisetzungsprofilen bereitzustellen. Durch pharmazeutische Optimierungsprozesse reformulieren wir gezielt Moleküle mit hohem therapeutischem Potenzial und eröffnen so neue Behandlungsperspektiven, die das Potenzial haben, die medizinische Versorgung grundlegend zu verändern.
Gemeinsame Entwicklung
AMW agiert als verlässlicher ‚Single Source‘-Anbieter für die Entwicklung neuer Lösungen zur Wirkstoffabgabe. Unser Geschäftsansatz beinhaltet das Aufsetzen und die Betreuung von Co-Entwicklungsprojekten, die das gesamte Spektrum von der Grundlagenforschung bis zur GMP-konformen Produktion klinischer Muster und marktfähiger Produkte abdeckt. Um einen nahtlosen Projektfortschritt sicherzustellen, setzen wir auf einen kooperativen Projektansatz, der durch effizientes und nachhaltiges Projektmanagement sorgfältig koordiniert wird. Dies ermöglicht kundenspezifische und kundenfokussierte Lösungen in allen Entwicklungsphasen.
Angepasste Herstellungslösungen (Contract Development and Manufacturing Organisation, CDMO)
Für Partner, die einzigartige Expertise und erstklassige Produktionsmöglichkeiten für biologisch abbaubare Implantatformulierungen suchen, stellt AMW maßgeschneiderte Fertigungsdienstleistungen zur Verfügung. Nach einem reibungslosen Transfer des Produktionsprozesses gewährleisten wir eine umfangreiche und zertifizierte Skalierung des Herstellungsablaufs. Dies erfolgt in GMP-konformen Produktionsstätten unter strikten Qualitätskontrollbedingungen, um in jeder Entwicklungsstufe ein Höchstmaß an Produktqualität zu sichern.
Nachhaltige Pipeline
mRNA-eluierendes bioabbaubares Implantat als Gentherapie der nächsten Generation. Prototyping und Plausibilitätsstudien abgeschlossen.
Gebrauchsfertiger Goserelin-Applikator im Zulassungsverfahren für Lateinamerika
Biologisch abbaubares Implantat für die intravitreale Anwendung, das über einen Zeitraum von sechs Monaten einen Wirkstoff freisetzt. Einsatzgebiete sind die Behandlung der altersbedingten Makuladegeneration (AMD), diabetischen Retinopathie und des Netzhautvenenverschlusses.
Entwicklung eines biologisch abbaubaren Implantats zur Abgabe von GLP-1-Agonisten, indiziert zur Behandlung des metabolischen Syndroms. Für den Wirkstoff liegen erfolgsversprechende Ergebnisse aus Machbarkeits- und humanen Pharmakokinetik-Studien vor.
Entwicklung eines biologisch abbaubaren Implantats zur Abgabe von GLP-1-Agonisten, indiziert zur Behandlung des metabolischen Syndroms. Die Machbarkeitsstudie ist in Kürze zu erwarten.
Vertraulich